遷移金属触媒反応の開発では、高度な立体選択性制御を達成できるよう反応条件の最適化に取り組んでいます。立体異性体の作り分けに有効であることから、高立体選択性の追求だけではなく、触媒による相補的な立体化学制御も視野に入れ、研究を進めています。
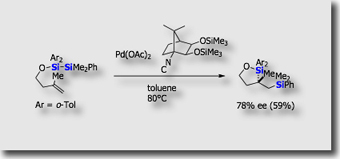
立体相補的分子内シリルホウ素化
環形成を伴うボリル化反応において、触媒上の配位子を適切に選択することにより立体選択性が制御可能な、興味深い反応系をいくつか見出しています。一つ目の例として、白金触媒によるアルケンの分子内シリルホウ素化を示します。[Ref.1] この反応では、PCyPhSUB{2};を配位子に有する白金触媒を用いるとtrans体の環状生成物を選択的に与えるのに対して、かさ高いトリアリールホスファイトを配位子に用いるとcis体が選択的に生成します。生成物の炭素ーホウ素結合を1炭素ホモログ化および酸化することにより、1,3,5-トリオールの両方のジアステレオマーを作り分けることができました。
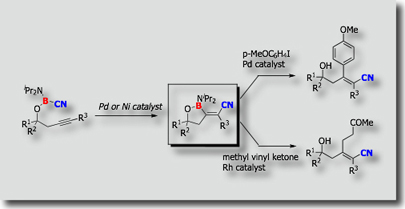
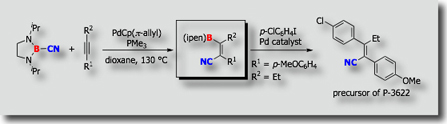
トランスメタル化環化カルボホウ素化
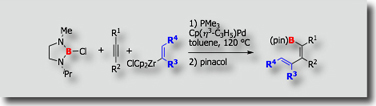
二つ目の例として、パラジウム触媒による環形成を伴うカルボホウ素化を示します。[Ref.2] この反応では、PMeSUB{3};を配位子に有するパラジウム触媒を用いるとcis付加体が高選択的に生成するのに対し、PCySUB{3};やP(t-Bu)SUB{3};やPPhSUB{3};を配位子に用いるとtrans付加生成物を選択的に得ることができます。
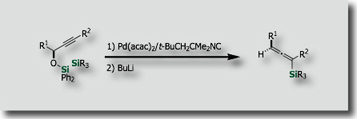
立体特異的カチオン性1,2-シリルシフト
有機ケイ素化合物の立体選択的または立体特異的分子変換と有機合成への応用にも精力的に取り組んでいます。例えば、アルキンの分子内ビスシリル化により生成した1,2-シロキセタンが、高立体特異的にカチオン性1,2-シリルシフトを起こし、プロパルギルシランを与えることを明らかにしました。[Ref.3] これにより、カチオン性syn [1,2] シリル転位が立体化学を保持して進行することが初めて示されました。
関連研究
- ビスシリル化
- 触媒的不斉ビスシリル化
- シリルホウ素化
- シリルホウ素化C–Cカップリング反応
- 分子内シアノホウ素化
- 触媒的不斉シリルホウ素化
- シアノシリル化 (Link to references)
- 分子内シアノホウ素化
- シアノホウ素化
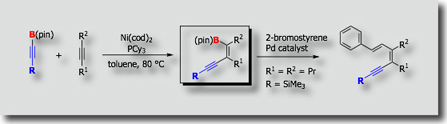
- アルキニルホウ素化
- トランスメタル化環化カルボホウ素化
- トランスメタル化3成分カルボホウ素化
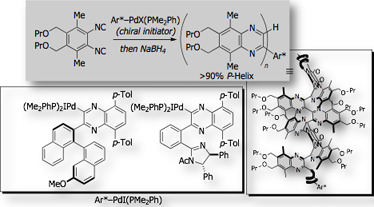
- 不斉重合
参考文献
- Ref. 1
- Ligand-Controlled, Complementary Stereoselectivity in the Platinum-Catalyzed Intramolecular Silaboration of Alkenes T. Ohmura, H. Furukawa, M. Suginome, J. Am. Chem. Soc. 2006, 128, 13366-13367, 10.1021/ja065588
- Ref. 2
- Palladium-Catalyzed trans- and cis-Carboboration of Alkynes Tethered to Chloroborane with Organozirconium Reagents: Ligand-Dependent Complementary Stereoselectivity M. Daini, A. Yamamoto, M. Suginome, J. Am. Chem. Soc. 2008, 130, 2918-1919, 10.1021/ja711160h
- Ref. 3
- Stereospecific Cationic [1,2]-Silyl Shift with Retention of Configuration at the Migrating Terminus M. Suginome, A. Takama, Y. Ito,J. Am. Chem. Soc. 1998, 120, 1930-1931, 10.1021/ja9737937