Current Research †Semi-wet Supramoleular Gel Group (超分子セミウェットデバイスの機能創成) † 我々のグループでは、「超分子セミウェットデバイスの機能創成」を目標に研究を行っています。 1.超分子ヒドロゲル † 図1
我々は、新規セミウェットデバイスとして超分子ヒドロゲルを開発しています。共有結合で架橋された高分子ヒドロゲルとは異なり、超分子ヒドロゲルでは、水中で分子間相互作用(疎水性相互作用、水素結合等)を協同的に働かせることで、階層的に自己集合し、疎水ドメインを有するファイバー構造が構築されます。そのファイバー同士が互いに絡まりあい網目状になった部位に水分子が捕らえられることで、ドライな固体ではなくウェットな液体でもない、その中間体であるゲル状態(“semi-wet”な環境)を形成することが可能となります。 2.Combinatorial screeningを利用した超分子ヒドロゲル化剤の開発 †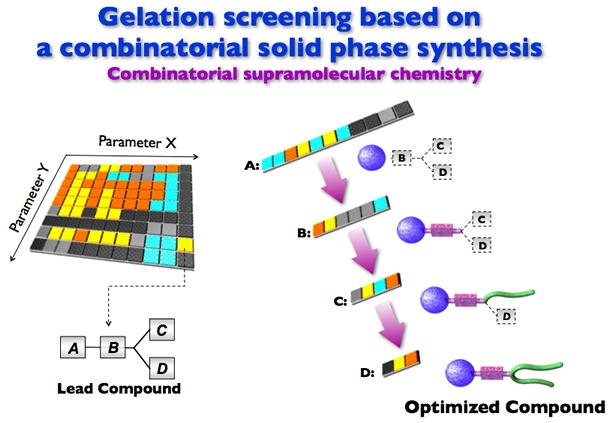 図2
我々は、世界で初めて超分子ヒドロゲル化剤のコンビナトリアルスクリーニングを可能とする固相合成法の開発に成功しました(SPLS 法)。その結果、超分子ヒドロゲル化剤を高収率で容易に合成でき、また、1人の研究者でもバラエティに富んだヒドロゲル化剤開発が可能となりました。 参考文献
3.刺激応答性ヒドロゲル化剤の開発 †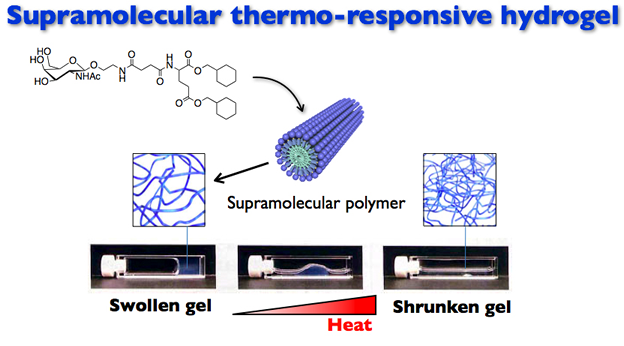 図3
超分子ヒドロゲル化剤のスクリーニングにより得られた複数のヒドロゲル化剤のうち、数種類のヒドロゲル化剤は、熱応答性体積相転移を有するゲルを形成することを発見しました。熱応答性体積相転移とは、室温では膨潤した状態のゲルが、温度を徐々に上げていくとある温度を境にゲルの体積が急激に収縮する現象のことを言います。この現象を利用し、“DNA の放出コントロール”や環境汚染物質である“ビスフェノールA の包摂除去”に成功しました。 参考文献
 図4
糖を親水ヘッドとする超分子ヒドロゲル化剤とpH 応答性官能基としてカルボキシル基を親水ヘッドとする添加剤を混合することで、超分子コポリマーが得られます。この超分子コポリマーはpH に依存して体積相転移することを発見しました。 参考文献
 図5
光応答性官能基としてフマル酸アミドをスペーサー部に有する超分子ヒドロゲル化剤の開発に成功しました。得られた超分子ヒドロゲルは紫外光照射に応答してゲルーゾル転移を起こすことが明らかになりました。 参考文献
4.超分子ヒドロゲル化剤を用いたナノバイオマテリアル †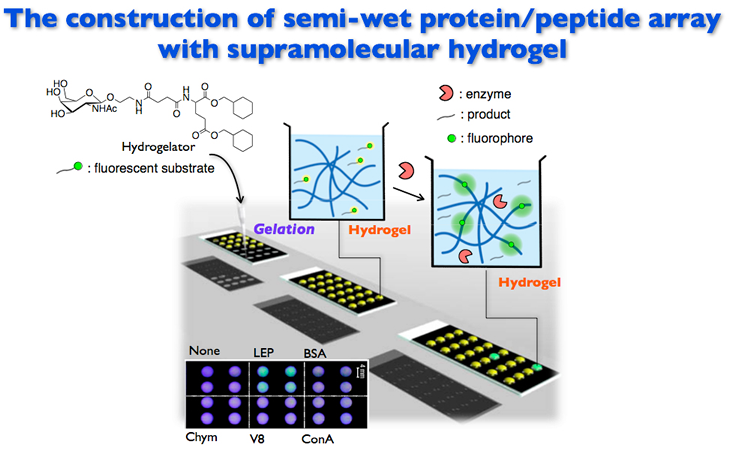 図6
当研究室で開発された超分子ヒドロゲル化剤により形成したヒドロゲルは“新規セミウェット型タンパク・ペプチドアレイの構築”にも展開されています。タンパク質の機能解明は、生命現象を理解する上で直接的な情報を与えます。そのため、近年、タンパク質機能をハイスループットに検出可能なプロテインチップ開発が行われています。中でも、ヒドロゲルをマトリックスとするチップは、基質及びタンパクをプレート上に固定化する必要がなく、また乾燥に強いため、従来の二次元チップでは困難であった“セミウェット状”のより自然な状態を作り出せます。 参考文献
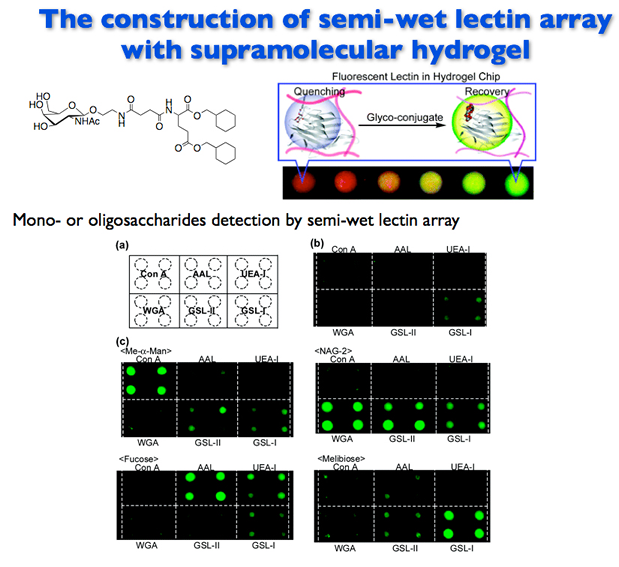 図7
高い選択性で糖鎖を認識するレクチンに蛍光色素を修飾し、消光剤を用いた検出システム(Biomolecular Fluorescence Quenching and Recovery: BFQR)を超分子ヒドロゲル中に内包したセミウェットレクチンアレイの構築に成功しました。糖鎖の違いをパターンから見分けることが可能となり、細菌や細胞に特徴的な糖鎖プロファイリング解析も行なえるようになりました。糖鎖はプロテオグリカンなどの形で細胞表層に存在し、細胞の分化・増殖あるいは毒素やウイルスの感染に関与しており、セミウェットレクチンアレイは細胞の性質や機能の解析あるいは感染の診断や治療薬の開発にも重要であると考えられます。 参考文献
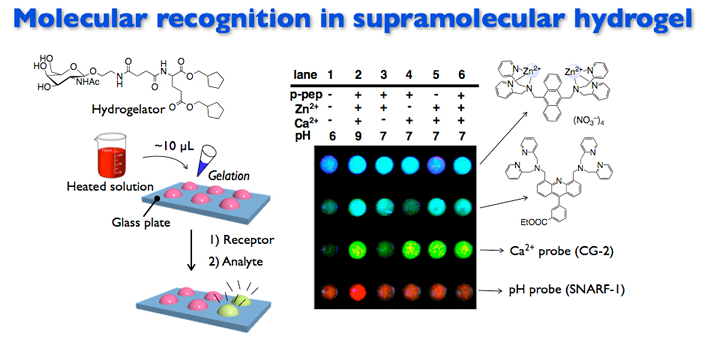 図8
広範な生理活性物質のセンシングには、多種類のセンサーやレセプターのアレイ化が求められています。我々の研究室で開発したリン酸アニオン応答性センサーや、pH や金属に応答するレセプターをヒドロゲルに内包することでセミウェット人工レセプターアレイの構築に成功しました。超分子ナノファイバーの疎水場を利用することで、環境応答性蛍光色素を修飾したレセプターによる疎水性の異なるリン酸アニオン種の識別も可能性であることが示されており、水中におけるハイスループットな生理活性物質検出等の応用が期待されます。 参考文献
 図9
光応答性超分子ゲル化剤を用いて、フォトマスクを利用したゾルーゲルパターニングに成功しました。レーザー光を集光することによってマイクロレベルのパターニングも可能であり、マイクロ反応場等としての応用が期待されます。 参考文献
 図10
刺激応答性超分子ゲル化剤を用いることで、熱・光によるバイオマテリアル(バクテリアやF1-ATPase(分子モータータンパク質))の運動制御が可能となりました。超分子組織体によるバイオマテリアルのマニピュレーションに関する可能性が示されました。 参考文献
|
添付ファイル:
View Edit
![[logo] [logo]](wiki/image/logo.png)